近日,国际著名期刊Angewandte Chemie International Edition(IF:16.823)在线发表了我校理学院张晓进教授课题组题为“A Carbon-Carbon Bond Cleavage–Based Prodrug Activation Strategy Applied to β-Lapachone for Cancer-Specific Targeting”的最新研究成果。博士研究生龚琪杰为本论文的第一作者,张晓进教授为本文的独立通讯作者,中国药科大学为本文的唯一作者及通讯单位。
前药是药物分子设计的重要策略。现有前药策略往往是通过“碳-杂键”(如C-O、C-N键)化学修饰来屏蔽原药结构中的羟基、羧基、氨基等活性基团,所形成的前药分子可在体内经“碳-杂键”断裂释放原药而发挥药效。邻醌类抗肿瘤药物的“邻醌”结构既是药效基团,又是介导副作用的毒性基团。由于“邻醌”结构中缺乏上述可修饰基团,难以通过常规手段设计化学稳定的前药分子。
本研究发展了一种基于“C-C键”断裂的前药设计策略:通过“C-C键”化学修饰来稳定屏蔽“邻醌”活性基团,设计合成获得α-羟基酮结构的前药分子;该前药分子还含有苯硼酸结构的ROS响应基团,可在肿瘤组织高水平ROS触发下,通过基于1,6-消除的“C-C键”断裂及快速氧化级联过程,选择性在肿瘤组织中释放邻醌类抗肿瘤药物。密度泛函理论(DFT)计算表明,关键的C-C键断裂释药步骤的活化能仅为8.3 kcal/mol,可在生理条件下快速释药,其驱动力可能源自产物的芳构化效应。作者将该前药策略应用于多个邻醌类抗肿瘤天然产物,代表性的β-lap前药分子具有良好体内抗胰腺癌药效,且在810 mg/kg剂量下对正常组织无明显毒副作用,安全性显著优于原药(LD50 = 115.8 mg/kg)。该研究发展的基于C-C键断裂的前药策略,为邻醌类药物的前药设计、改善安全性等提供了新方法与新思路。
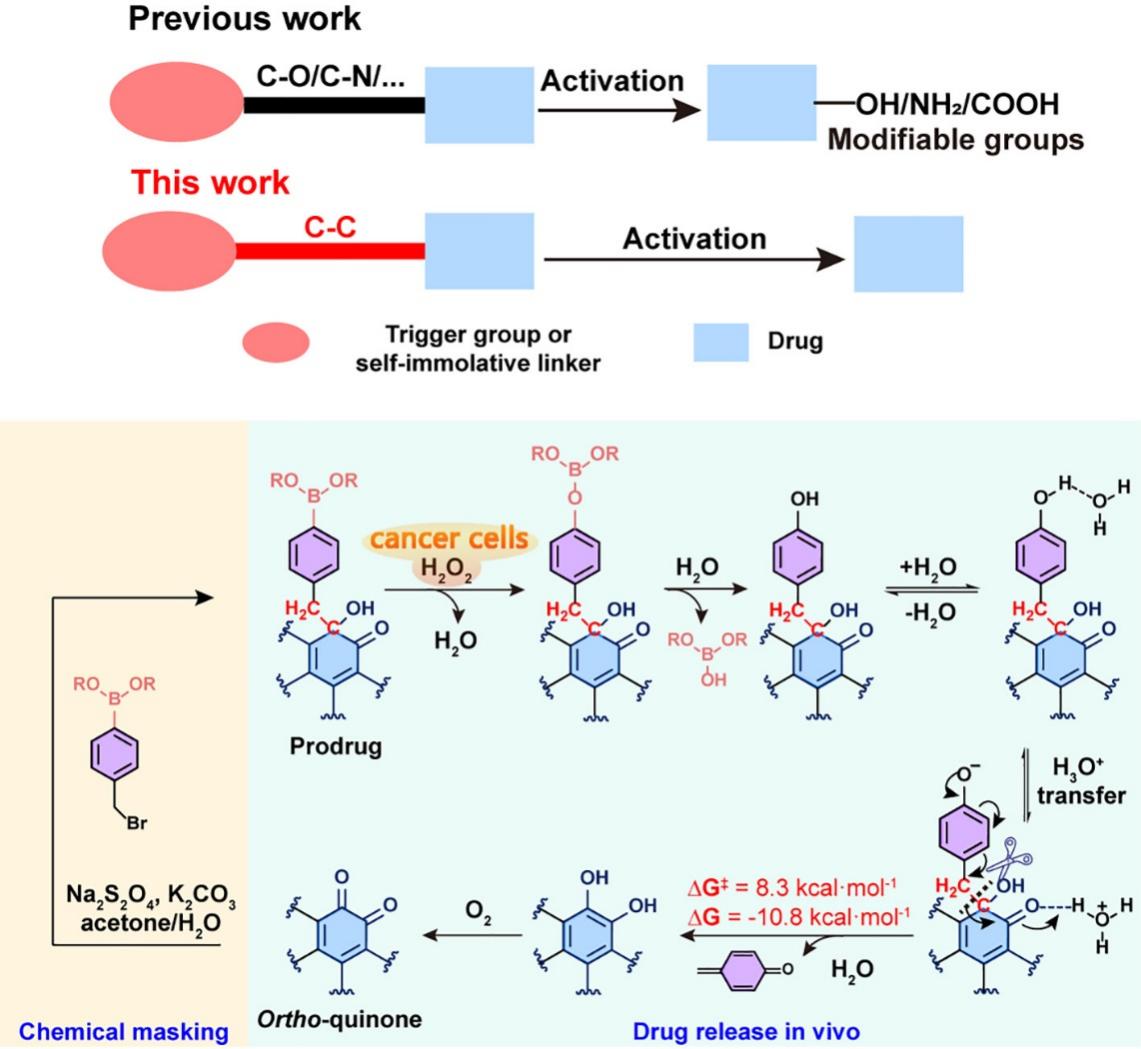
图1 基于“C-C键”断裂的邻醌前药设计策略
该研究工作得到江苏省杰出青年基金、国家自然科学基金面上项目、中国药科大学兴药学者计划等资助以及江苏省药物分子设计与成药性优化重点实验室的支持。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202210001
(供稿单位:理学院,撰写人:王亚茹,审稿人:黄欣、郑诗翌)





